Thu hồi thuốc chứa chất gây ung thư do Trung Quốc sản xuất trên toàn quốc
Theo thông báo của Cơ quan quản lý dược phẩm châu Âu (EMA), Cơ quan quản lý dược Canada và một số cơ quan quản lý dược khác, các thuốc chứa Valsartan được sản xuất từ nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical-Trung Quốc sản xuất buộc phải thu hồi. Nguyên nhân là do nguyên liệu này chứa tạp chất N-nitrosodimethylamine (NDMA) có nguy cơ gây ung thư.
Tại Việt Nam, valsartan được nhiều công ty nhập từ Trung Quốc để sản xuất thuốc và ghi tên thương hiệu khác nhau. Cục Quản lý dược (Bộ Y tế) ghi nhận có 23 loại thuốc trên thị trường trong nước chứa thành phần valsartan nguy cơ ung thư.
Theo đó, để đảm bảo an toàn cho người sử dụng, Cục Quản lý Dược yêu cầu Sở y tế các tỉnh, thành phố trực thuộc Trung ương, các cơ sở sản xuất, kinh doanh thuốc đình chỉ lưu hành tất cả các thuốc thành phẩm được sản xuất từ nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical - Trung Quốc sản xuất.
Ảnh: Vietq
Các công ty đăng ký thuốc, sản xuất thuốc, công ty nhập khẩu cần phối hợp với các nhà phân phối thuốc thông báo thu hồi tất cả các lô thuốc thành phẩm trong công thức sản xuất có chứa nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical - Trung Quốc sản xuất theo danh mục kèm theo tới các cơ sở bán buôn, bán lẻ, sử dụng thuốc.
Đồng thời, Cục yêu cầu ngừng ngay việc sử dụng nguyên liệu này để sản xuất thuốc thành phẩm; thực hiện đánh giá nhà cung cấp, kiểm tra, nghiên cứu sử dụng nguyên liệu Valsartan của nhà sản xuất mới nhằm đảm bảo yêu cầu về chất lượng, an toàn cho người sử dụng và thực hiện thủ tục thay đổi hồ sơ đăng ký thuốc theo đúng qui định của pháp luật. Các công ty gửi báo cáo thu hồi về Cục Quản lý Dược trong vòng 1 tháng kể từ ngày ký công văn này. Theo đó, hồ sơ thu hồi bao gồm: Số lượng xuất xưởng, số lượng thu hồi và các bằng chứng về việc thực hiện thu hồi tại các cơ sở bán buôn, bán lẻ, sử dụng đã mua thuốc theo qui định của Bộ Y tế.
Ngoài ra, Cục Quản lý Dược cũng yêu cầu: Các cơ sở đăng ký thuốc phối hợp với các cơ sở sản xuất có tên trong danh sách kèm theo báo cáo khẩn về nguồn gốc của nguyên liệu Valsartan sử dụng trong sản xuất các loại thuốc có chứa Valsartan lưu hành tại Việt Nam. Các cơ sở nhập khẩu thuốc, nguyên liệu làm thuốc báo cáo tình hình nhập khẩu, phân phối liên quan đến nguyên liệu nói trên. Dừng nhập khẩu, cung cấp thuốc đã được sản xuất từ nguyên liệu này.
Danh sách đình chỉ lưu hành tất cả các thuốc thành phẩm được sản xuất từ nguyên liệu Valsartan do Công ty Zhejiang Huahai Pharmaceutical của Trung Quốc sản xuất cụ thể như sau:
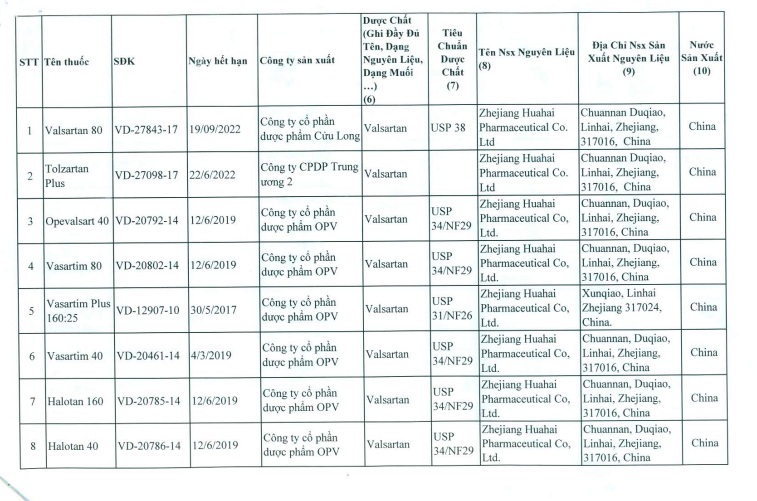
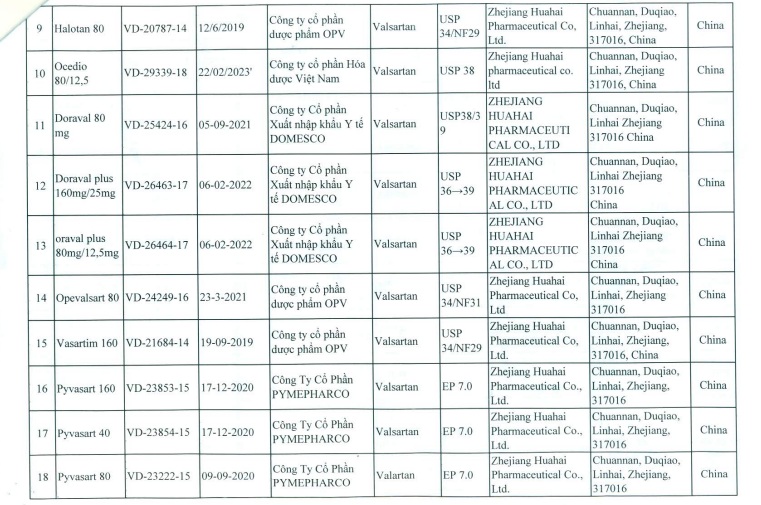
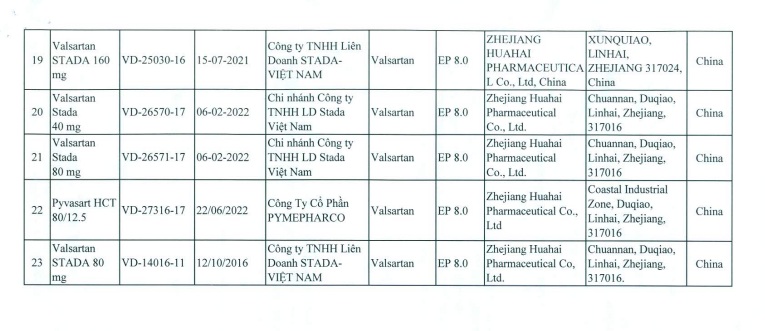
- Cảnh báo: Thuốc chống ung thư vú tamoxifen làm tăng nguy cơ mắc ung thư cổ tử cung ở phụ nữ
- Nissan thừa nhận gian lận khí thải với hơn 1000 xe ô tô
- Tiêu hủy số lượng lớn chim và gà nhập lậu tại Quảng Ninh
Vân Trà(t/h)






